Complete Guide to TEV Protease Processing and Ni Spin Column Purification
TEV Protease 처리와 Ni Spin Column 정제 가이드
MBP-tag 단백질 정제를 할 때 많은 연구자들이 선택하는 시스템이 바로 pMAL-c6T 벡터입니다. 이 시스템을 활용하면 MBP-tag와 표적 단백질을 효율적으로 분리할 수 있고, 특히 TEV protease를 이용한 절단 과정과 이후 Ni Spin Column을 통한 분리 단계는 높은 순도의 단백질을 확보하는 데 매우 중요합니다.
이번 포스트에서는 TEV 처리 후 정제 단계별로 버퍼 교환이 필요한지 여부, 단백질 손실의 원인, 그리고 실험 중 확인 방법(SDS-PAGE)까지 꼼꼼히 안내드릴게요.
TEV protease 처리 시 버퍼 교환은 필요할까?
많은 분들이 궁금해하시는 것 중 하나는, amylose resin에서 elution한 단백질 용액에 TEV protease를 처리하기 전 버퍼 교환이 필요한지입니다.
정답은 NO!
Amylose 컬럼의 elution buffer는 TEV protease의 반응 버퍼와 매우 유사하기 때문에, 10X TEV buffer를 따로 첨가하지 않고도 바로 반응시킬 수 있습니다.
또한 TEV 반응물 자체를 Ni Spin Column에 그대로 로딩해도 무방합니다.
단백질 구조와 정제 흐름 요약
pMAL-c6T 벡터를 사용하는 경우 단백질 구성은 다음과 같습니다:
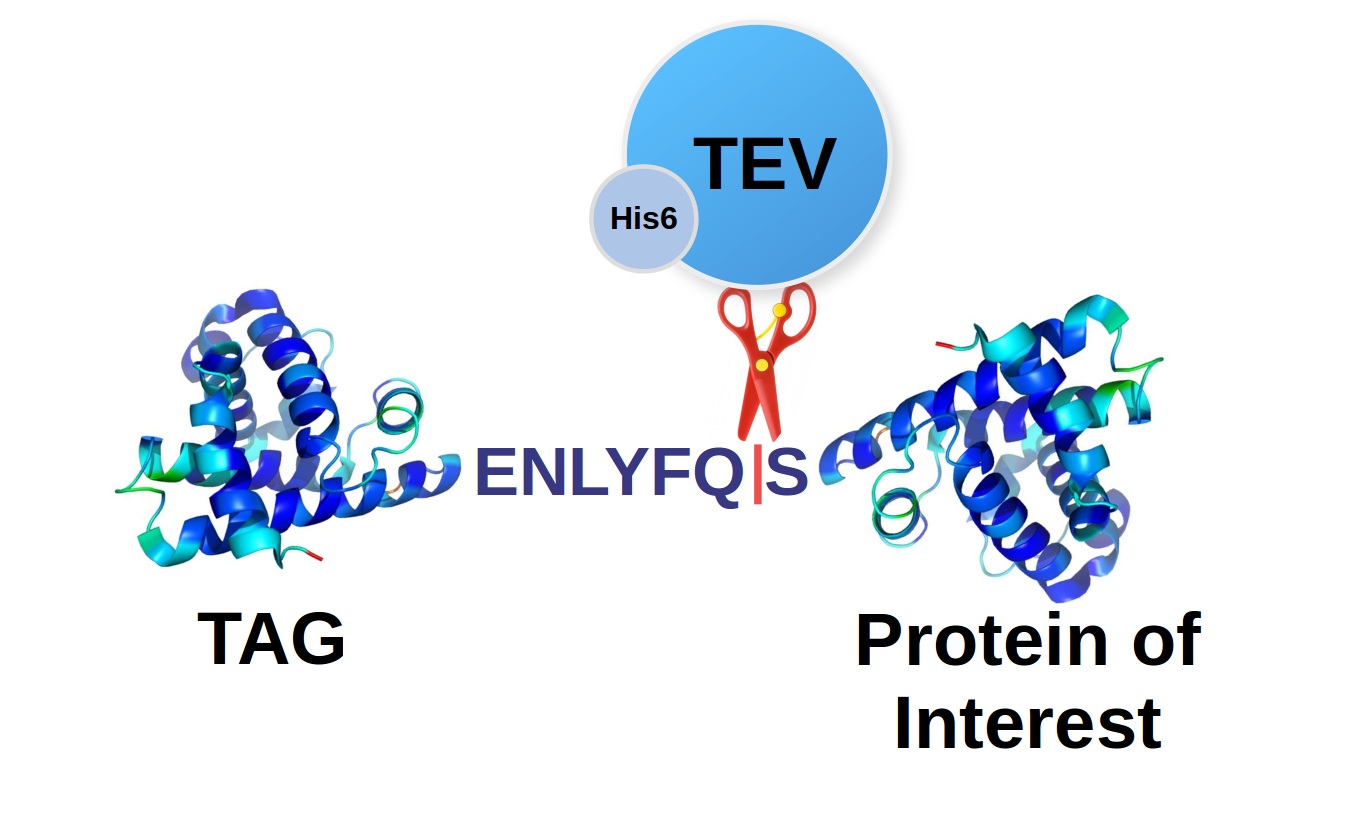
HHHHHH-MBP-linker (TEV protease 절단 서열 포함)-표적 단백질
이 구조의 단백질을 amylose resin에서 정제한 후, His-tag를 갖는 TEV protease로 처리하면 다음과 같은 결과물이 생성됩니다:
- HHHHHH-MBP-linker (절단 서열 포함)
- 표적 단백질
이 혼합물을 Ni Spin Column에 로딩하면:
- His-tag를 가진 TEV protease와 MBP-linker는 Ni resin에 결합
- 표적 단백질은 flow-through로 분리
Ni Column 이후 단백질이 손실되는 경우
간혹 기대했던 만큼 표적 단백질이 flow-through에서 확인되지 않거나 손실될 수 있습니다. 이럴 때 고려해볼 수 있는 원인은 다음과 같습니다:
1. 단백질 침전
TEV 처리 후 표적 단백질이 불안정해져 침전되었을 가능성
2. Ni resin과의 비특이 결합
표적 단백질에 His-like motif가 존재하거나 히스티딘 잔기가 많아 Ni resin에 강하게 결합한 경우
→ 이 경우, imidazole 농도가 높은 buffer로 elution해야 회수 가능합니다.
실험적으로 확인하는 방법: SDS-PAGE
표적 단백질이 손실되었는지 확인하려면?
elution 후 남은 resin 일부를 SDS 로딩 버퍼에 섞고, SDS-PAGE를 돌려보세요.
→ Resin에 남은 단백질 존재 여부를 직접 눈으로 확인할 수 있습니다.
실험 요약 정리
| 단계 | 작업 내용 | 주의사항 |
|---|---|---|
| Step 1 | Amylose resin 정제 | Elution buffer는 TEV 반응에 바로 사용 가능 |
| Step 2 | TEV protease 처리 | 별도 10X buffer 없이 가능 |
| Step 3 | Ni Spin Column 로딩 | 표적 단백질은 flow-through에서 회수 |
| Step 4 | 침전/결합 확인 | SDS-PAGE로 resin 확인 필요 |
마무리 요약
- 버퍼 교환 필요 없음: amylose elution → TEV 처리 → Ni Column까지 한 번에 가능
- 표적 단백질은 flow-through에 존재: His-tag 없는 구조이기 때문
- 손실 발생 시 침전 또는 비특이 결합 의심
- SDS-PAGE로 확인 필수